Аметов А.С., Карпова Е.В.
В настоящее время в мире сахарным диабетом
(СД) болеют минимум 285 млн человек, и к 2030 г. эта цифра, вероятно,
составит более 438 млн [1]. Важно отметить, что в десятку стран, в
которых наибольшее число людей страдают СД, помимо Индии, Китая, США,
Индонезии, Японии, Пакистана, Бразилии, Италии, Бангладеша, в настоящее
время входит и Россия [2]. По данным Государственного регистра больных
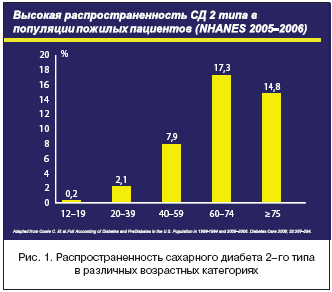
СД на 1 января 2010 г., в России насчитывается более 3,1 млн пациентов с СД, из которых 2 822 634 – с СД 2–го типа. Однако данные контрольно–эпидемиологических исследований ФГУ ЭНЦ Росмедтехнологий в рамках федеральной программы «Сахарный диабет»; показали, что реальная распространненость заболевания составляет около 9 млн человек. Известно, что наибольшее количество пациентов с наиболее распространенным типом СД (2–й тип) составляют люди пожилого возраста (рис. 1). По данным эпидемиологических исследований ФГУ ЭНЦ, распространенность СД 2–го типа увеличивается с возрастом и составляет 8% у лиц старше 60 лет [1].
Не вызывает сомнений, что речь идет о тяжелом и прогрессирующем
заболевании, связанном с развитием как микрососудистых, так и
макрососудистых осложнений диабета. Достаточно тревожным является тот факт, что СД 2–го типа
занимает 3–е место среди непосредственных причин смерти после
сердечно–сосудистых и онкологических заболеваний, которые также наиболее
часто встречаются у людей среднего и старшего возраста. По
статистическим данным, каждые 6–7 пациентов из 10 погибают от макроангиопатических осложнений диабета.
Причем наряду с распространенностью СД нарастают и
социально–экономические потери, связанные с развитием тяжелых
инвалидизирующих осложнений.
Однако хорошо известно, что лидирующее место в структуре заболеваемости и смертности у пациентов
с СД 2–го типа занимают все же именно макрососудистые осложнения [3].
Так, риск развития ишемической болезни сердца (ИБС) при СД 2–го типа
возрастает в 2–5 раз, а риск развития мозговых инсультов – в 3–4 раза,
смертность от ИБС, по данным разных источников, – в 3–6 раз, а от
цереброваскулярных заболеваний в 2–3 раза превышает аналогичные
показатели в общей популяции [4]. Помимо этого, при СД 2–го типа имеет
место и высокая распространенность микрососудистых осложнений. Риск
развития терминальной нефропатии с хронической почечной недостаточностью
(ХПН) при СД возрастает в 15–20 раз, потери зрения вследствие
пролиферативной ретинопатии – в 10–25 раз, гангрены – в 15 раз [5–7].
Развитие осложнений связывают в первую очередь с хронической
гипергликемией, что было убедительно доказано в ходе длительных
крупномасштабных исследований, в том числе UKPDS (United Kingdom
Prospective Diabetes Study). Очевидно, что единственным способом
предотвратить или отсрочить развитие грозных осложнений СД является
ранняя диагностика заболевания и строгий самоконтроль с поддержанием
показателей уровней глюкозы крови, максимально приближенных к
физиологическим, без повышения риска гипогликемии и без ущерба для
качества жизни пациентов. Поэтому ученые во всем мире
занимаются поиском новых лекарственных средств для более эффективного и
безопасного управления этим заболеванием.
Известно, что СД является гетерогенным заболеванием, развивающимся в
результате комбинации врожденных и приобретенных факторов. В настоящее
время наличие генетической основы для развития этого заболевания не
вызывает никаких сомнений. Риск развития СД 2–го типа возрастает от 2 до
6 раз при наличии диабета у родителей или ближайших
родственников. Однако генетика этого заболевания достаточно сложна и,
очевидно, речь идет о комбинированном расстройстве.
Необходимо отметить, что у большинства пациентов с СД 2–го типа и наличием гипергликемии отмечаются:
– инсулинорезистентность;
– нарушенная секреция инсулина;
– повышение продукции глюкозы печенью;
– изменения секреции и действия инкретинов.
Данные патологические процессы усугубляются с возрастом. Как правило,
инсулинорезистентность прогрессирует, соответственно, снижается захват
глюкозы периферическими тканями, что может зависеть от степени
генетического вклада и/или приобретенных состояний, таких как ожирение,
малоподвижный образ жизни и старение. Лица старшего возраста обычно
предпочитают, в силу тех или иных причин, калорийную пищу с избыточным
содержанием насыщенных жиров и легко усваиваемых углеводов. Многим
приходится принимать множество различных препаратов по поводу
сопутствующих заболеваний, которые негативно влияют на углеводный обмен.
Также сопутствующие заболевания ограничивают пожилых
людей в физической активности, что в совокупности с рядом других
факторов (такими как гормональный дисбаланс, гликозилирование белков,
снижение запасов витаминов и развитие анемии и др.) приводит к
существенному снижению мышечной массы [1].
Наиболее значительные изменения отмечаются в плане снижения функции
β–клеток и нарушения секреторной способности инсулина. Известно, что
секреция инсулина у человека, в зависимости от физиологического смысла,
делится на 3 типа:
• базальная секреция;
• пульсовая секреция;
• двухфазная секреция.
Базальная секреция в физиологических условиях выполняет роль фундамента,
имеющего место даже в отсутствие экзогенных стимулов в течение 24 ч с
периодичностью 80–150 мин. Она контролирует различные механизмы действия
инсулина в плане гомеостаза глюкозы, обеспечивает баланс между
скоростью продукции глюкозы печенью и периферическим захватом глюкозы
глюкозозависимыми тканями в течение ночи и длительного периода между
приемами пищи, а также удерживает продукцию глюкозы печенью в состоянии
равновесия с базальной утилизацией глюкозы головным мозгом и другими
тканями.
Пульсовая секреция инсулина занимает от 8 до 14 мин., четко коррелируя с
колебаниями уровней С–пептида. Интерес представляют данные о том, что
при определении совпадений пиков секреции инсулина с пиками глюкозы у
здоровых лиц они совпадали в 80–85% случаев, а у больных СД 2–го типа
только в 46% случаев [8].
Известно, что в ответ на внутривенное введение глюкозы секреция инсулина
происходит в 2 фазы: первая длится в среднем в течение 10 мин.,
характеризуется наличием острых пиков; вторая длится в среднем 60–120
мин., характеризуется постепенным повышением выделения инсулина. Следует
отметить, что первая фаза необходима для эффективного контроля за
постпрандиальной гликемией.
Важно отметить, что у людей пожилого возраста без
наличия избыточного веса происходит снижение первой фазы секреции
инсулина. Существуют убедительные данные, что у людей после 50 лет
каждое десятилетие происходит повышение уровня постпрандиальной гликемии
на 0,5 ммоль/л.
В многочисленных исследованиях показано, что с возрастом продукция
глюкозы печенью существенно не меняется; также не изменяется влияние
инсулина на продукцию глюкозы печенью [1].
В последние годы большой научно–практический интерес вызывает изучение
роли гормонов желудочно–кишечного тракта в регуляции секреции инсулина, а
следовательно, и в регуляции гомеостаза глюкозы в организме человека,
так как регуляция гомеостаза глюкозы в организме осуществляется сложной
мультигормональной системой, включающей гормоны не только поджелудочной
железы, но и гормоны–инкретины, вырабатываемые в кишечнике в ответ на
прием пищи [9]. Доказано, что после приема глюкозы внутрь наблюдается
более выраженное увеличение секреции инсулина по сравнению с тем,
которое происходит после внутривенной инфузии глюкозы, сопровождающейся
идентичным повышением уровня гликемии. Этот эффект назван «эффектом
инкретина» и свидетельствует о большой значимости сигналов
желудочно–кишечного тракта в гормональной регуляции гомеостаза глюкозы. В
настоящее время существует мнение, что постпрандиальная секреция
инсулина примерно на 70% обусловлена потенцирующим эффектом инкретинов,
продуцируемых эндокриноподобными клетками желудочно–кишечного тракта
[10]. У лиц пожилого возраста инкретиновая секреция
остается в пределах нормальных значений. Однако стало известно, что с
возрастом наблюдается значительное снижение чувствительности β–клеток
поджелудочной железы к действию инкретинов.
Учитывая все изменения регуляции углеводного обмена, происходящие с
возрастом, становится понятна тенденция к увеличению заболеваемости СД
2–го типа у пожилых лиц. Лечение пожилых пациентов
нередко вызывает определенные сложности. Следует отметить, что в
настоящее время необходимо применять индивидуальный подход к выбору целей терапии
СД 2–го типа, особенно у лиц старшей возрастной группы. Доказано, что
сердечно–сосудистые осложнения и смертность чаще встречаются у пациентов
с нередкими эпизодами гипогликемии. Поэтому совет экспертов Российской
ассоциации эндокринологов рекомендует при выборе цели терапии
учитывать возраст пациента с СД 2–го типа или «ожидаемую
продолжительность жизни» (рис. 2), а также наличие тяжелых осложнений
заболевания, риск развития тяжелой гипогликемии. По данным исследования
VADT, перенесенная тяжелая гипогликемия в 4 раза повышает риск
сердечно–сосудистой смертности и по значимости превосходит другие
факторы риска [11]. Следует отметить, что у пожилых пациентов более
низкий порог гипогликемии, поэтому время для самостоятельного
купирования эпизода гипогликемии ограничено, а следовательно,
увеличиваются риски тяжелой нейрогликопении, после которой могут
возникнуть транзиторные ишемические атаки и транзиторная гемиплегия
[12]. Помимо этого представляют особый интерес данные, что риск
переломов шейки бедра достоверно выше у больных с регулярными
гипогликемиями, что в первую очередь связано с частыми падениями во
время эпизодов резкого снижения уровня сахара крови [1].
В последнее десятилетие благодаря фундаментальным и клиническим
исследованиям развилось новое и перспективное направление в лечении СД
2–го типа, основанное на использовании эффекта инкретинов. Поскольку
период полужизни ГПП–1 очень короткий, в клинической
практике его невозможно использовать в качестве натурального препарата. В
связи с этим было предложено ингибирование фермента ДПП–4, разрушающего
естественные инкретины организма. Основным преимуществом сахароснижающей терапии,
основанной на инкретиновом эффекте, является низкий риск развития
гипогликемии, что наиболее значимо у пожилых пациентов, а также
нейтральное влияние на массу тела.
Одними из представителей являются препараты Галвус (вилдаглиптин) и
ГалвусМет (вилдаглиптин + метформин). Комбинированная форма лекарства
особенно удобна у лиц старшей возрастной группы, поскольку позволяет
снизить количество принимаемых препаратов и достичь лучшей
приверженности терапии. Препараты Галвус и ГалвусМет досконально изучены в международной клинической практике, так как исследования по их оценке начались более 6 лет назад.
Данные международных исследований доказали, что терапия
препаратами Галвус и ГалвусМет является высокоэффективной и безопасной.
Она обеспечивает достижение целей гликемического контроля без
осложнений и побочных эффектов. В Европе вилдаглиптин – единственный ингибитор
ДПП–4, не имеющий ограничения в терапии очень пожилых пациентов.
Галвус можно комбинировать с любым сахароснижающим препаратом, в том
числе и с инсулином [13].
Данные клинических исследований доказали и
продемонстрировали возможность назначения препаратов Галвус и ГалвусМет
на всех этапах терапии диабета, в том числе и на старте терапии после
установления диагноза.
В 2011 г. опубликованы данные 24–недельного исследования, в котором изучалась терапия вилдаглиптином у пациентов с СД 2–го типа старше 75 лет. В группе пациентов старше 75 лет, принимавших вилдаглиптин
в монотерапии, отмечалось значимое снижение уровня гликированного
гемоглобина (HbA1c) в среднем на 0,9% по сравнению с более молодыми
пациентами без увеличения риска развития гипогликемии и на 1,1% при
приеме вилдаглиптина в комбинации с другими сахароснижающими препаратами (рис. 3) [14].
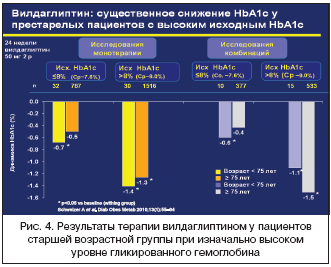
Помимо этого изучалась эффективность терапии при высоких значениях
уровня HbA1c. У пациентов с показателем HbA1c более 8,0% снижение уровня
гликемии происходит более значимо во всех возрастных категориях (рис.
4).
V. Fonseca и соавт. в одной из своих научных работ (2006) изучали эффективность добавления вилдаглиптина
(50 мг/сут.) к инсулину (средняя суточная доза составляла 82 ед.) у 256
больных с неудовлетворительными показателями углеводного обмена
(исходно уровень HbA1с в среднем составлял 8,4%) в течение 24 нед. На
протяжении периода исследования режим инсулинотерапии у пациентов не
менялся. К концу наблюдения значения уровня HbA1с в основной группе
снизились на 0,5%, в группе контроля (инсулин в сочетании с плацебо) –
всего на 0,2%. Интересно отметить, что у больных в возрасте от 65 лет и
старше комбинация инсулина с вилдаглиптином способствовала уменьшению
уровня HbA1с на 0,7%, в то время как в контрольной группе статистически
значимой разницы по возрасту не отмечено (рис. 5).
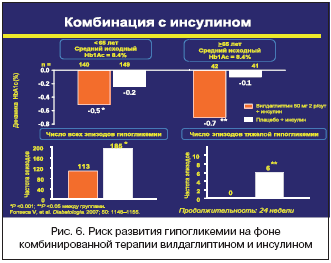
Также необходимо отметить, что эпизоды гипогликемии регистрировались
существенно реже в основной группе, что, вероятно, обусловлено
повышением чувствительности α–клеток поджелудочной железы к глюкозе
(рис. 6) [15].
Таким образом, появление ингибиторов ДПП–4 (в частности
вилдаглиптина) существенно облегчает задачу эффективного и безопасного
управления СД 2–го типа у пациентов старшей возрастной группы.
Ингибиторы ДПП–4 не вызывают развитие гипогликемий, не обладают
кардио–, гепато– и нефротоксичностью, хорошо переносятся (отсутствие
нежелательных явлений со стороны желудочно–кишечного тракта), не влияют
на массу тела, а также удобны в применении (1 или 2 раза/сут. в зависимости от клинической ситуации).



Литература
1. Дедов И.И., Шестакова М.В. Сахарный диабет в пожилом возрасте: диагностика, клиника, лечение. Практическое руководство для врачей. Москва. –2011.
2. Garcia–Caballero M., Tinahones F.J., Cohen R.V. Diabetes surgery – 2010 – Р. 140–141.
3. Niskanen L, Turpeinen A, Penttila I, Uusitupa MI. Hyperglycemia and
compositional lipoprotein abnormalities as predictors of cardiovascular
mortality in type 2 diabetes: a 15–year follow–up from the time of
diagnosis. Diabetes Care 1998; 21 (11):1861–1869.
4. Stratton JM, Adler AI, Neil AW, et al. Association of glycaemia with
macrovascular and microvascular complications of type 2 diabetes (UKPDS
35): prospective, observational study. BMJ.2000; 321:405–412.
5. Stratton JM, Adler AI, Neil AW, et al. Association of glycaemia with
macrovascular and microvascular complications of type 2 diabetes (UKPDS
35): prospective, observational study. BMJ.2000; 321:405–412.
6. Дедов И.И. Шестакова М.В. Сахарный диабет. М., Универсум Паблишинг, 2003г., с. 231–242;244–256;263–267, 282–289.
7. Дедов И.И. Шестакова М.В. Диабетическая нефропатия. М., Универсум Паблишинг, 2000г., с.239.
8. Аметов А.С. Физиология метаболизма глюкозы.//А.С.Аметов, Сахарный диабет 2 типа: проблемы и решения, 2011, стр.21–51.
9. А.С. Аметов. Регуляция секреции инсулина в норме и при сахарном
диабете 2 типа: роль инкретинов. РМЖ – 2006 – т.14 – №26 – С.1867–1872.
10. А.С.Аметов, Е.В.Карпова. Инкретиномиметики – новый этап в лечении
сахарного диабета 2–го типа, РМЖ, ТОМ 18, №23 (387), 2010, стр.
1410–1415.
11. Дедов И.И., Шестакова М.В., Аметов А.С., Анциферов М.Б., Галстян
Г.Р., Майоров А.Ю., Петунина Н.А., Сухарева О.Ю. Проект «Консенсус
совета экспертов Российской ассоциации эндокринологов (РАЭ) по инициации
и интенсификации сахароснижающей терапии сахарного диабета 2
типа».//Сахарный диабет. –2011.–№1.–С.98–108.
12. А.С. Аметов, Е.В. Иванова. Гипогликемия.//А.С.Аметов, Сахарный диабет 2 типа: проблемы и решения, 2011, стр.115–143.
13. King H, Aubert RE, Herman WH. Global burden of diabetes, 1995–2025:
prevalence, numerical estimates, and projections. Diabetes Care 1998;
1414–1431.
14. Schweizer A., Dejager S., Foley J.E., Shao Q., Kothny W. Clinical
experience with vildagliptin in the management of type 2 diabetes in a
patient population ≥ 75 years: a pooled analysis from a database of
clinical trials. Diabetes, Obesity and Metabolism 13(1):55–64, 2011.
15. Fonseca V., Dejager S., Albrecht S. et al. Vildagliptin as add–on to
insulin in patients with type 2 diabetes (T2DM). Diabetes 2006;
55(suppl 1):A111.



 Cлучайное видео:
Cлучайное видео:


