Мелешкевич Т.А., Лучина Е.И., Лукашова М.Е.
В настоящее время сахарный диабет (СД) является
одним из наиболее распространенных эндокринных заболеваний. По прогнозам
Всемирной Организации Здравоохранения, число больных СД в мире к 2030
году увеличится до 366 млн человек.
СД – это серьезная медико–социальная проблема. Неуклонный рост
заболеваемости, инвалидизация, «почетное» третье место среди
непосредственных причин смерти. Благодаря этому ситуацию с диабетом можно смело назвать эпидемией неинфекционного заболевания. Среди эндокринной патологии сахарный диабет
занимает первое место по распространенности (более 50% от всех
эндокринных заболеваний). Более 230 миллионов человек в мире страдает диабетом, что составляет уже 6% взрослого населения мира. Смерть по причине диабета и его осложнений
происходит каждые 10 секунд. Диабет уносит более 3 млн. жизней в год. К
2025 г. самую большую группу больных в развивающихся странах составят
пациенты зрелого, наиболее работоспособного возраста.
Сосудистые осложнения СД являются причиной ранней
инвалидизации и высокой летальности. Смертность от болезней сердца и
инсульта у больных СД в 2–3 раза, слепота в 10 раз, нефропатия в 12–15
раз, а гангрена нижних конечностей почти в 20 раз чаще, чем среди
населения в целом. Дополнительными факторами риска заболеть СД являются
ожирение, гиподинамия, атеросклероз, гипертоническая болезнь. Каждые 30
секунд в мире производится ампутация нижних конечностей по причине
диабета, причем значительное количество больных только после операции
узнают, что у них был сахарный диабет. Среди основных причин развития поздних осложнений
СД ведущее место занимает нарушение внутриклеточного метаболизма и
феномен оксидативного стресса, в связи с чем все большее внимание
уделяется препаратам, обладающим антиоксидантным действием. Наиболее
известным и широко применяемым препаратом в данной группе является актовегин, который представляет собой высокоочищенный гемодиализат, получаемый методом ультрафильтрации из крови телят. Актовегин
содержит аминокислоты, олигопептиды, нуклеозиды, продукты углеводного и
жирового обмена, липиды, олигосахариды, электролиты и микроэлементы.
В нескольких экспериментальных исследованиях было установлено, что по характеру действия актовегин
сходен с инсулином. Этот факт был подтвержден Parade с соавт.,
описавшими его инсулиноподобное действие в отношении захвата глюкозы
жировыми клетками у крыс. Авторы пришли к выводу, что актовегин
содержит вещества – инозитолфосфоолигосахариды (IPO), обладающие
инсулиноподобным действием. В итоге была предложена двухступенчатая
модель действия IPO, предполагающая как повышение активности
переносчиков глюкозы в цитоплазматической мембране, так и прямое
увеличение транспорта глюкозы в клетку. Таким образом, существуют как
прямые, так и косвенные данные в пользу существования у актовегина
инсулиноподобного действия, которое отличается от действия самого
инсулина преимущественным влиянием на переносчики глюкозы, а не на
увеличение ее потока. Тем не менее конечным итогом действия служит
повышение утилизации глюкозы, напрямую влияющее на метаболизм клеток и
баланс энергии в тканях. Еще одним интересным вопросом является скорость
воздействия актовегина на поступление энергии в клетку: Schwabe
показал, что актовегин в значительной степени активирует внутриклеточные
окислительные процессы и ускоряет не только энергетический, но и
резервный метаболизм (что в случае сердца и печени сопровождается
усиленным накоплением гликогена и калия). Таким образом, актовегин,
обладая инсулиноподобным действием и стимулируя клеточный метаболизм,
повышает потребление кислорода и выработку энергии. Эти эффекты
описаны в различных органах и тканях, что подтверждает представление об
актовегине, как стимуляторе, поддерживающем работу тканей, нуждающихся в
поступлении энергии. Поэтому в будущем представляется интересным
выяснить, может ли восполнение запасов энергии и кислорода в тканях
усилить также рост и репликацию клеток.
Эта гипотеза изучалась в исследованиях о влиянии актовегина на
заживление ран. В согласии с описанными выше результатами находится
недавно проведенное двойное слепое многоцентровое рандомизированное контролируемое клиническое исследование по изучению эффективности и безопасности актовегина у больных СД 2 типа с клинически значимой диабетической полинейропатией (ДПН). Лечение
привело к значительному ослаблению нарушений чувствительности и
снижению порога вибрационной чувствительности с отчетливой тенденцией к
достоверности различий по сравнению с группой плацебо.
В Германии было проведено исследование под руководством Martin Elmlinger по изучению эффектов
актовегина in vitro. Целью исследования было: изучение механизма
действия актовегина в лабораторных условиях (исследовались клетки
эмбрионов крыс), а точнее, влияние препарата на рост клеток,
выживаемость и устойчивость к оксидативному стрессу. Кроме того,
оценивалось воздействие актовегина на клетки крыс с диабетической
полиневропатией и со стрептоцидиндуцированным диабетом. Результатами
исследования стало: дозозависимое увеличение количества нейронов и
стимуляция деления клеток; уменьшение концентрации активных форм
кислорода (АФК) после введения актовегина у лабораторных животных на
фоне оксидативного стресса, вызванного тетро-бутил-гидропероксидом.
Приведенные данные экспериментальных и клинических исследований, а также
накопленный к настоящему времени опыт подтверждают целесообразность
применения актовегина в лечении осложнений СД, особенно связанные с сочетанным поражением нервной ткани и сосудистыми нарушениями.
Врачебной аудитории известны данные плацебоконтролируемых многоцентровых
исследований актовегина у пациентов с ДПН. Еще в 1987 году W. Jansen и
E. Beck опубликовали результаты исследования по эффективности
применения таблетированной формы актовегина в дозе 1800 мг/сут у
пациентов с СД 2 типа и ДПН. В группе, получавшей актовегин, по
сравнению с плацебо наблюдалось достоверное снижение негативной и
позитивной неврологической симптоматики. Опыт данного исследования лег в
основу проведения более масштабного клинического исследования у
пациентов с СД и с ДПН, которое проводилось в 26 центрах России, Украины
и Казахстана. В исследование вошли 567 пациентов с СД 2 типа. Схема лечения
включала сначала 20 в/в инфузий актовегина по 2000 мг 1 раз в сутки,
затем прием актовегина в таблетированной форме в течение 140 дней.
Результаты исследования показали, что актовегин достоверно уменьшает
клнические проявления диабетической полиневропатии и улучшает качество
жизни больных СД 2 типа.
Давно известно положительное влияние актовегина на диабетическую
макроангиопатию, однако, к сожалению, на сегодняшний день не проведены
многоцентровые плацебо–контролируемые исследования, доказывающие
положительное влияние актовегина на ишемические поражения при СД.
Гурьева И.В. с соавт. одними из первых инициировали проведение такого
рода исследования о влиянии актовегина на нейроишемический болевой
синдром нижних конечностей при СД. Было проведено пилотное
рандомизированное открытое сравнительное 8–недельное исследование о
влиянии препарата на состояние ишемического синдрома нижних конечностей у
больных СД 2 типа по сравнению с сулодексидом. В исследование было
включено 26 пациентов. Лечение актовегином проводилось в
виде инфузий в дозе 2000 мг 1 раз в сутки с переходом на поддерживающий
прием актовегина 1200 мг/сут в 3 приема в течение 6 недель (всего 8
недель лечения). В результате этого исследования было
показано, что актовегин в течение 8 недель терапии достоверно
увеличивает дистанцию ходьбы у пациентов с перемежающей хромотой.
Кротовский Г.С., Зудин А.М., Учкин И.Г. с соавт. также оценивали влияние
актовегина на «критическую» ишемию нижних конечностей. В исследование
было включено 58 человек, которым проводился курс – 14 внутривенных
вливаний актовегина 8 мг/мл (2000 мг в сутки) по сравнению с плацебо.
После курса терапии по данным дуплексного сканирования определилось
статистически достоверное улучшение гемодинамики, улучшилось качество
жизни пациентов по опроснику SF–36, уменьшилась выраженность симптомов
критической ишемии нижних конечностей в группе актовегина по сравнению с
плацебо.
На базе эндокринологического отделения НУЗ ЦКБ № 2 имени Н.А. Семашко
ОАО «РЖД» было также проведено пилотное исследование возможности
воздействия актовегина на проявления диабетической полинейропатии и
диабетической макроангиопатии. Обследованы пациенты с СД 1 типа (4
человека) и 2 типа (32 человека) в возрасте от 27 до 72 лет с
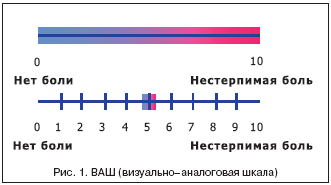
нейроишемическими поражениями нижних конечностей. Всем пациентам в
начале проводилась оценка неврологического статуса по шкалам ВАШ
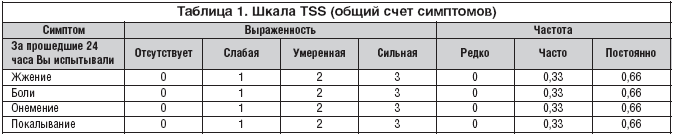
(визуально–аналоговая шкала) (рис. 1), TSS (табл. 1), НДС
(нейропатический диабетический счет), стимуляционная электромиография
(ЭМГ), допплеровское исследование сосудов нижних конечностей с
исследованием плече–лодыжечного индекса (ПЛИ), а также проводилась
оценка качества жизни при помощи опросника SF–36. Кроме того, всем
пациентам проводилось стандартное офтальмологическое обследование
глазного дна до и после лечения для оценки влияния актовегина на течение
диабетической ретинопатии. В исследование были включены пациенты с
уровнем ВАШ более 5, TSS свыше 6, НДС свыше 10, ПЛИ ниже 0,9. Курс
лечения составил 1000 мг в течение10 дней с последующим пероральным
приемом в течение 6 недель в дозе 1800 мг/сут в 3 приема.
Выраженность симптомов ДПН (боль, жжение, парестезии, онемение),
количественно оцениваемые с помощью шкалы TSS, значительно снизилась к
концу исследования – с 7,66±2,32 до 4,32±1,66 (p<0,005). Также порог
вибрационной, тактильной, температурной, болевой чувствительности,
определявшийся в 5 точках на ногах с помощью неврологических
инструментов с подсчетом НДС, достоверно уменьшился по сравнению с
первоначальным уровнем – с 15±5 до 12±4 (p<0,05). При оценке
результатов наблюдалось достоверное улучшение показателя ВАШ при
применении актовегина с 7±2 до 4±2 (p<0,005) в конце исследования.
В результате было показано улучшение позитивной и негативной
неврологической симптоматики, однако при проведении повторной ЭМГ в
конце исследования достоверных различий в сравнении с исходными данными
получено не было.
Отмечалось достоверное увеличение ПЛИ с 0,9±3 до 0,7±3 в конце
исследования (p<0,005), и что особенно важно – все пациенты отмечали
улучшение качества жизни согласно опроснику SF–36 (рис. 2).
Предметом особого наблюдения явилась диабетическая ретинопатия (ДР) до и
после лечения, т.к. многие препараты с выраженным сосудистым эффектом,
применяемые для лечения нейроишемического варианта синдрома
диабетической стопы, вызывают прогрессирование диабетической ретинопатии
и не могут быть применены при наличии пролиферативной стадии ДР. До
проведения курса лечения в 23% случаев была выявлена пролиферативная
диабетическая ретинопатия. После завершения исследования ухудшения
состояния глазного дна выявлено не было, однако и улучшения течения
диабетической ретинопатии также не обнаружено. Возможно, это связано с
коротким курсом лечения, и необходимо длительное проспективное
исследование по изучению влияния актовегина на течение диабетической
ретинопатии.
В результате лечения была подтверждена эффективность препарата для
лечения не только ДПН, но и диабетической макроангиопатии. В ходе
терапии побочных эффектов получено не было. Таким образом, данное
исследование показало, что лечение актовегином повышает качество жизни
пациентов с СД, страдающих ДПН в сочетании с ишемическими поражениями
нижних конечностей, а также безопасно и эффективно уменьшает
выраженность нейропатических симптомов, и достоверно снижает порог
сенсорной чувствительности, улучшает кровоток артерий нижних
конечностей, тем самым значительно снижая риск развития язвенных
поражений стоп.
В заключение хотелось бы отметить, что актовегин является одним из
препаратов выбора у пациентов с нейроишемическим поражением нижних
конечностей и пролиферативной диабетической ретинопатией.
Несомненно, эффективность препарата в терапии ишемических и
неврологических поражений при СД, в лечении диабетической ретинопатии
должна изучаться и далее.

Литература
1. Florian Buchmayer, Johannes Pleiner, Martin W. Elmlinger, Gereon
Lauer, Gertfried Nell, Harald H. Sitte// Actovegin: a biological drug
for more than 5 decades. 2011
2. Jansen W., Beck E. // Die Medizinische Welt. 1987. V. 38. P. 838.
3. Ziegler D, Movsesyan L, Mankovsky B, Gurieva I, Abylaiuly Z, Strokov
I. Treatment of Symptomatic Polyneuropathy With Actovegin in Type 2
Diabetic Patients. Diabetes Care. // August 2009 32:1479–1484.
4. Ziegler D, Rathmann W, Dickhaus T, Meisinger C, Mielck A, the KORA
Study Group. Prevalence of polyneuropathy in pre–diabetes and diabetes
is associated with abdominal obesity and macroangiopathy: the
MONICA/KORA Augsburg Surveys S2 and S3. Diabetes Care 2008; 31:464–469
5. И. А. Строков // Клинический опыт. Результаты плацебоконтролируемого
многоцентрового исследования «актовегин по сравнению с плацебо у
пациентов с диабетической полиневропатией». 2009.
6. Аметов А.С., Моргоева Ф.Э., Строков И.А. Диабетическая энцефалопатия и
полиневропатия: терапевтические возможности актовегина // Русский
медицинский журнал. №6. 2005.
7. Оболенский В.Н. Комплексное лечение больных с синдромом диабетической
стопы.// Опыт клинического применения актовегина в эндокринологии. М.,
2005.
8. Кротовский Г.С., Зудин А.Н., Учкин И.Г., Талов Н.А., Александрова
Е.С. // Медикаментозное лечение хронической ишемии нижних конечностей.
РМЖ. 2010. №17.
9. Гурьева И.В., Бегма И.В., Кузина И.В., Бегма А.Н., Светлова О.В.//
Патогенетическое лечение актовегином нейроишемического болевого синдрома
нижних конечностей при сахарном диабете. РМЖ. 2009. №10.



 Cлучайное видео:
Cлучайное видео:


